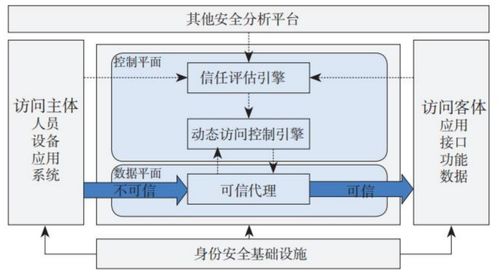
上海自贸试验区医疗器械注册人制度 为信息安全设备创新注入新动力
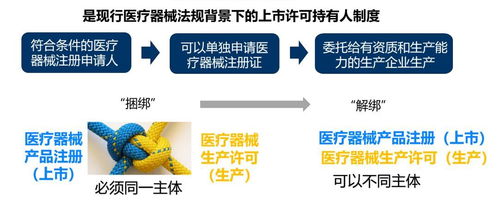
上海自贸试验区自实施医疗器械注册人制度以来,为整个医疗器械产业的创新研发与市场化进程带来了革命性的变化。这一制度的核心在于允许医疗器械注册申请人(即“注册人”)与生产主体分离,打破了传统模式下研发与生产必须捆绑的壁垒,显著降低了创新主体的准入门槛和运营成本。对于技术迭代迅速、安全要求极高的信息安全设备领域而言,这一制度更如同为其新产品问世铺设了一条高效的“快车道”。
一、 制度创新:破解研发与生产的耦合难题
传统的医疗器械监管要求产品注册证与生产许可证必须归属于同一主体,这使得许多拥有先进技术但缺乏规模化生产能力的高校、科研院所或初创企业望而却步。上海自贸试验区的注册人制度则允许“注册人”专注于产品研发、临床试验和上市后质量管理,而将生产环节委托给具备相应资质和生产能力的企业。这种专业化分工,使得信息安全设备这类高度依赖特定前沿技术(如加密算法、安全芯片、隐私计算框架)的产品,能够更快地将实验室成果转化为符合法规要求的商品。
二、 聚焦信息安全设备:驶入创新“快车道”的具体体现
信息安全设备,如医疗数据加密传输设备、安全隔离与信息交换系统(网闸)、医疗物联网终端安全防护设备等,是保障智慧医疗、远程诊疗健康发展的关键基础设施。在注册人制度下,其创新优势尤为凸显:
- 加速技术转化:专注于网络安全的科技公司可以轻资产运营,无需自建厂房即可委托成熟的医疗器械制造商生产其硬件设备,大大缩短了从原型机到量产产品的周期。
- 激发创新活力:制度降低了初创企业的前期投入风险,鼓励更多社会资本和智力资源投入医疗信息安全设备的研发,催生出更多针对新型医疗场景(如可穿戴设备数据安全、云影像平台防护)的解决方案。
- 优化资源配置:优质的生产资源得以在全行业共享,避免了重复建设。注册人可以遴选全国乃至全球最合适的代工厂,促进产业链上下游的协同与专业化水平提升。
- 强化全生命周期管理:制度明确了注册人对产品全生命周期质量安全的主体责任,倒逼其在设计开发、供应链管理、上市后监测等环节建立更严谨的体系。这对于需要持续应对网络威胁的信息安全设备而言,意味着从源头建立了更可靠的安全质量管控闭环。
三、 监管协同与未来展望
制度的顺利运行离不开严谨的跨区域监管协同。上海药监部门与受托生产企业所在地监管部门建立了高效的衔接、检查和责任追究机制,确保“放得开”的同时也“管得住”。随着制度的不断完善和推广,预计将有更多融合了人工智能、区块链等技术的创新型医疗信息安全设备借助这一“快车道”快速上市,为构建安全可信的医疗健康数字生态提供坚实支撑。
总而言之,上海自贸试验区的医疗器械注册人制度,通过深刻的制度创新,不仅简化了产品上市流程,更从根本上重塑了医疗器械产业的创新生态。对于正处风口的医疗信息安全设备产业,这无疑是一次关键的赋能,推动中国在医疗科技与信息安全交叉的尖端领域,驶向全球创新的前沿。
最新产品